Cours de physique – niveau classe de première S – partie « Lois et modèles – Cohésion et transformations de la matière »
- Qu’est-ce qu’un alcane ? Définition
- Formule générale d’un alcane
- Nomenclature : terminaison du nom d’un alcane
- Nomenclature : nom de la chaîne principale
- Nomenclature : nom des substituants
- Nomenclature : numérotation des carbones de la chaîne principale
- Nomenclature : position des substituants
- Nomenclature : cas des alcanes cycliques
- Nom et formules des principaux alcanes
Qu’est-ce qu’un alcane ? Définition
Définition
Un alcane est une espèce chimique faisant partie de la famille des hydrocarbures, il est composé exclusivement d’atome d’hydrogène (H) et de carbone (C) liés entre eux uniquement par des liaisons simple (pas de liaisons multiples).
Les alcanes sont donc les espèces organiques les plus simples, ils en possèdent les éléments de base (carbone) mais excluent toute fonction chimique ainsi que les liaisons doubles ou triples.
Remarque
Les espèces chimiques ayant la même structure que les alcanes mais intégrant une ou plusieurs doubles liaisons font partie de famille des alcènes. Celles comprenant une ou plusieurs liaisons triples font partie de la famille des alcynes.
Formule générale d’un alcane
Un alcane étant composé uniquement de carbone (formant chacun 4 liaisons simples) et d’hydrogène (formant chacun une liaison simple) il est possible de prévoir la formule générale d’un alcane. Un alcane non cyclique comprenant un nombre “n” (entier) de carbone sera toujours associé à un nombre 2.n +2 d’hydrogène par conséquent sa formule brute sera de la forme :
CnH2n+2
Exemples
- alcane à 1 carbone, 2.1 + 2 = 4 soit la formule CH4
- alcane à 2 carbone, 2.2 + 2 = 6 soit la formule C2H6
- alcane à 3 carbone, 2.3 + 2 = 8 soit la formule C3H8
- alcane à 4 carbone, 2.4 + 2 = 10 soit la formule C4H10
Dans le cas d’un alcane cyclique, la fermeture de la chaîne fait intervenir deux liaisons carbone qui ne peuvent plus être consacrées à des hydrogène d’où la formule générale suivante:
CnH2n
Nomenclature : terminaison du nom d’un alcane
Le nom d’un alcane possède toujours une terminaison en “ane”.
Exemples: méthane propane, heptane etc
Réciproquement si le nom d’une espèce chimique se termine par “ane” alors il s’agit d’un alcane.
Nomenclature : nom de la chaîne principale
Définition
La chaîne principale d’un alcane correspond au plus long enchaînement direct de carbone.
Exemples
Dans les formules semi-développées suivantes les carbone de la chaîne principale sont représentés en rouge
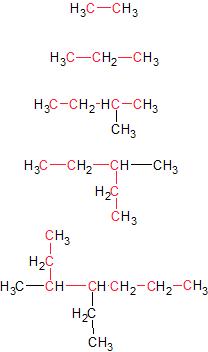
Le nom, de la chaîne principale dépend du nombre de carbone qu’elle comporte. À chaque nombre de carbone correspond un préfixe qui, une fois associé à la terminaison en “ane”, constitue le nom de l’alcane.
Préfixes des alcanes comportant de 1 à 9 carbone:
| Nombre de carbone dans la chaîne principale | Préfixe du nom de l’alcane |
| 1 | meth- |
| 2 | éth- |
| 3 | prop- |
| 4 | but- |
| 5 | pent- |
| 6 | hex- |
| 7 | hept- |
| 8 | oct- |
| 9 | non- |
Préfixe des alcanes comportant 10 à 19 carbone
| Nombre de carbone dans la chaîne principale | Préfixe du nom de l’alcane |
| 10 | déc- |
| 11 | undéc- |
| 12 | dodéc- |
| 13 | tridéc- |
| 14 | tetradéc- |
| 15 | heptadec- |
| 16 | hexadec- |
| 17 | heptadec |
| 18 | octodec |
| 19 | nonadec |
Préfixe des alcanes comportant plusieurs dizaines de carbone
| Nombre de carbone dans la chaîne principale | Préfixe du nom de l’alcane |
| 20 | eicos- |
| 30 | triacont- |
| 40 | tetracont- |
| 50 | pentacont- |
| 60 | hexacont- |
| 70 | heptacont- |
| 80 | octacont- |
| 90 | nonacont- |
| 100 | hect- |
A partir de la vingtaine d’atomes le nombre de carbone intermédiaire entre deux dixaine est indiqué par un préfixe supplémentaire:
- hen pour 1
- do pour 2
- tri pour 3
- tetra pour 4
- penta pour 5
- hexa pour 6
- hepta pour 7
- octa pour 8
- nona pour 9
Exemples
- un alcane linéaire à 32 carbones (30 +2) est du dotriacontane (do pour 2 et triacont pour la trentaine)
- un alcane linéaire à 58 carbone (50 + 8) est de l’octapentacontane
Nomenclature : nom des substituants
Définition
Les substituant sont tout les groupements ne faisant pas partie pas partie de la chaîne principale.
Dans les exemples suivants la chaîne principale est en rouge tandis que les substituants sont en verts:
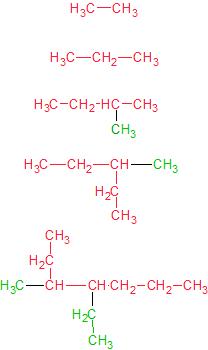
Le nom d’un substituant dépend de son nombre de carbone, il est formé du même préfixe que les la chaine principale mais associée à une terminaison en -yle.
Aini, par exemple:
- Un substituant à un carbone (-CH3) se nomme méthyle
- Un substituant à deux carbone ( -CH2-CH3) se nomme éthyle
- Un substituant à trois carbone ( -CH2-CH2-CH3) se nomme propyle
etc
Nom des substituant linéaires comportant de un à neuf carbone
| Nombre de carbone du subtsituant | nom de du substituant |
| 1 | methyle |
| 2 | éthyle |
| 3 | propyle |
| 4 | butyle |
| 5 | pentyle |
| 6 | hexyle |
| 7 | heptyle |
| 8 | octyle |
| 9 | nonyle |
Nomenclature : numérotation des carbones de la chaîne principale
Afin de préciser l’emplacement des substituants sur la chaîne principale il est nécessaire de numéroter les carbone de cette chaîne. Il faut donc choisir l’un des carbone situé à un bout de la chaîne pour être le numéro 1 tandis que celui situé à l’autre extrémité sera le carbone de numéro le plus élevée.
Les règles pour choisir la numérotation sont les suivantes:
- L’ensemble des indices doit être le plus faible possible
- Dans le cas de substituant différents occupant de positions équivalente la priorité est donné au premier dans l’ordre alphabétique.
Exemples de numérotation des carbones de la chaîne carbonée:
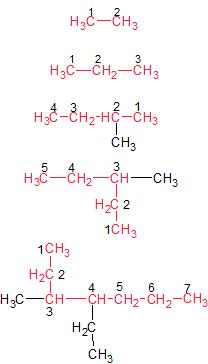
Nommenclature : position des substituants
La position d’un substituant correspond au numéro du carbone de la chaîne principale par lequel il est porté:
- Un substituant lié au carbone n°2 est en position 2
- Un substituant lié au carbone n°3 est en position 3 etc
Dans le nom de l’alcane, le nombre correspondant à la position est indiqué devant (à gauche) du nom du substituant dont il est séparé par un tiret moyen
Exemples
- si une chaîne principale hexane porte un seul substituant méthyle sur son carbone n°2 alors son nom complet est 2-méthylhexane.
- si une chaîne principale heptane port un seul substituant éthyle sur son carbone n°3 alors son nom complet est 3-éthylheptane.
Si un même substituant se répète plusieurs fois alors:
- ses différentes positions sont toutes indiquées, séparées par des virgules
- le nom du substituant est précédé du prfixe “di” s’il se répètre deux fois, “tri” s’il se répète trois fois et “tétra” s’il se répète quatre fois.
Exemples
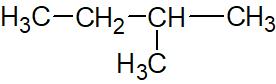
Il y a un substituant méthyle en position 2, cet alcane se nomme donc 2-méthylbutane
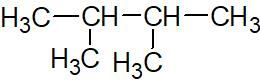
Il y a un substituant méthyle en position 2 et un autre en position 3, cet alcane se nomme donc 2,3-diméthylbutane
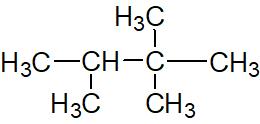
Il y a deux substituant méthyle en position 2 et un autre en position 3, cet alcane se nomme donc 2,2,3-triméthylbutane
S’il y a plusieurs types substituants alors ils sont indiqué dans l’ordre alphabétique
Exemples
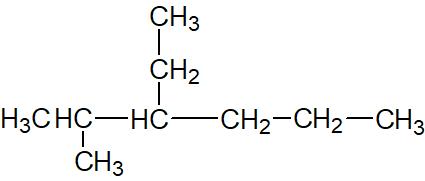
Cet alcane est le 3-ethyl-2-méthylhexane
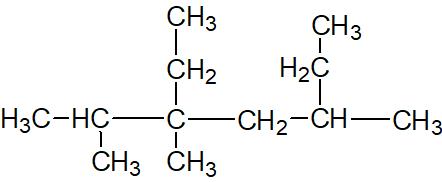
Cet alcane est le 3-ethyl-2,3,5-trimethylheptane
Nomenclature : cas des alcanes cycliques
Les règles de nomenclure son presque les même que celle des alcanes linéaires aux exceptions suivante:
- le préfixe cyclo est ajouté devant le de la chaîne principale
- le cycle constitue la chaîne principale
- le carbone n°1 est choisi de manière à minimiser les indices de l’ensemble des substituants
Exemple
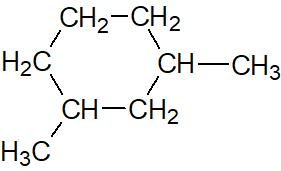
Le 1,3-dimethylcyclohexane
Nom et formules des principaux alcanes
|
Nombre de carbone |
Nom de l’alcane linéaire non ramifié |
|
|---|---|---|
| 1 | CH4 | méthane |
| 2 | C2H6 | éthane |
| 3 | C3H8 | propane |
| 4 | C4H10 | butane |
| 5 | C5H12 | pentane |
| 6 | C6H14 | hexane |
| 7 | C7H16 | heptane |
| 8 | C8H18 | octane |
| 9 | C9H20 | nonane |
| 10 | C10H22 | décane |
| 11 | C11H24 | undécane |
| 12 | C12H26 | dodécane |
| 13 | C13H28 | tridécane |
| 14 | C14H30 | tétradécane |
| 15 | C15H32 | pentadécane |
| 16 | C16H34 | hexadécane |
| 17 | C17H36 | heptadécane |
| 18 | C18H38 | octadécane |
| 19 | C19H40 | nonadécane |
| 20 | C20H42 | eicosane |
| 21 | C21H44 | heneicosane |
| 22 | C22H46 | docosane |
| 23 | C23H48 | tricosane |
| 24 | C24H50 | tétracosane |
| 25 | C25H52 | pentacosane |
| 26 | C26H54 | hexacosane |
| 27 | C27H56 | heptacosane |
| 28 | C28H58 | octacosane |
| 29 | C29H60 | nonacosane |
| 30 | C30H62 | triacontane |
| 31 | C31H64 | hentriacontane |
| 32 | C32H66 | dotriacontane |
| 33 | C33H68 | tritriacontane |
| 34 | C34H70 | tétratriacontane |
| 35 | C35H72 | pentatriacontane |
| 36 | C36H74 | hexatriacontane |
| 37 | C37H76 | heptatriacontane |
| 38 | C38H78 | octatriacontane |
| 39 | C39H80 | nonatriacontane |
| 40 | C40H82 | tétracontane |
| 41 | C41H84 | hentétracontane |
| 42 | C42H86 | dotétracontane |
| 43 | C43H88 | tritétracontane |
| 44 | C44H90 | tétratétracontane |
| 45 | C45H92 | pentatétracontane |
| 46 | C46H94 | hexatétracontane |
| 47 | C47H96 | heptatétracontane |
| 48 | C48H98 | octatétracontane |
| 49 | C49H100 | nonatétracontane |
| 50 | C50H102 | pentacontane |
| 51 | C51H104 | henpentacontane |
| 52 | C52H106 | dopentacontane |
| 53 | C53H108 | tripentacontane |
| 54 | C54H110 | tétrapentacontane |
| 55 | C55H112 | pentapentacontane |
| 56 | C56H114 | hexapentacontane |
| 57 | C57H116 | heptapentacontane |
| 58 | C58H118 | octapentacontane |
| 59 | C59H120 | nonapentacontane |
| 60 | C60H122 | hexacontane |
| 61 | C61H124 | henhexacontane |
| 62 | C62H126 | dohexacontane |
| 63 | C63H128 | trihexacontane |
| 64 | C64H130 | tétrahexacontane |
| 65 | C65H132 | pentahexacontane |
| 66 | C66H134 | hexahexacontane |
| 67 | C67H136 | heptahexacontane |
| 68 | C68H138 | octahexacontane |
| 69 | C69H140 | nonahexacontane |
| 70 | C70H142 | heptacontane |
| 71 | C71H144 | henheptacontane |
| 72 | C72H146 | doheptacontane |
| 73 | C73H148 | triheptacontane |
| 74 | C74H150 | tétraheptacontane |
| 75 | C75H152 | pentaheptacontane |
| 76 | C76H154 | hexaheptacontane |
| 77 | C77H156 | heptaheptacontane |
| 78 | C78H158 | octaheptacontane |
| 79 | C79H160 | nonaheptacontane |
| 80 | C80H162 | octacontane |
| 81 | C81H164 | henoctacontane |
| 82 | C82H166 | dooctacontane |
| 83 | C83H168 | trioctacontane |
| 84 | C84H170 | tétraoctacontane |
| 85 | C85H172 | pentaoctacontane |
| 86 | C86H174 | hexaoctacontane |
| 87 | C87H176 | heptaoctacontane |
| 88 | C88H178 | octaoctacontane |
| 89 | C89H180 | nonaoctacontane |
| 90 | C90H182 | nonacontane |
| 91 | C91H184 | hennonacontane |
| 92 | C92H186 | dononacontane |
| 93 | C93H188 | trinonacontane |
| 94 | C94H190 | tétranonacontane |
| 95 | C95H192 | pentanonacontane |
| 96 | C96H194 | hexanonacontane |
| 97 | C97H196 | heptanonacontane |
| 98 | C98H198 | octanonacontane |
| 99 | C99H200 | nonanonacontane |
| 100 | C100H202 | hectane |
Notions de seconde à réviser
Autres cours du thème “Lois et modèles – Cohésion et transformations de la matière“

Très bon récapitulatif vraiment même quelqu’un qui n’a jamais étudié ce cours en classe comprendrais
Très bon cours merci beaucoup, vraiment ça ma beaucoup servi